妊孕性/妊孕性温存について
男性の方へ
男性の生殖機能
はじめに

男性の生殖機能とは簡単にいいますとパートナー女性を妊娠させる機能ということになります。そしてその機能は卵子と融合する精子を作る機能(造精機能)と精液(精子)を尿道より射出して女性器内へ送り込む機能(性機能)に分けられます。この二つがあってはじめて自然な妊娠が可能になります。
この項ではこの二つの機能についてお話ししていきます。
精子を作る機能
ご存知かと思いますが、精子を作っているのは精巣(睾丸)です。1日あたりヒトは精子を150〜275×106個作ることができると言われています。
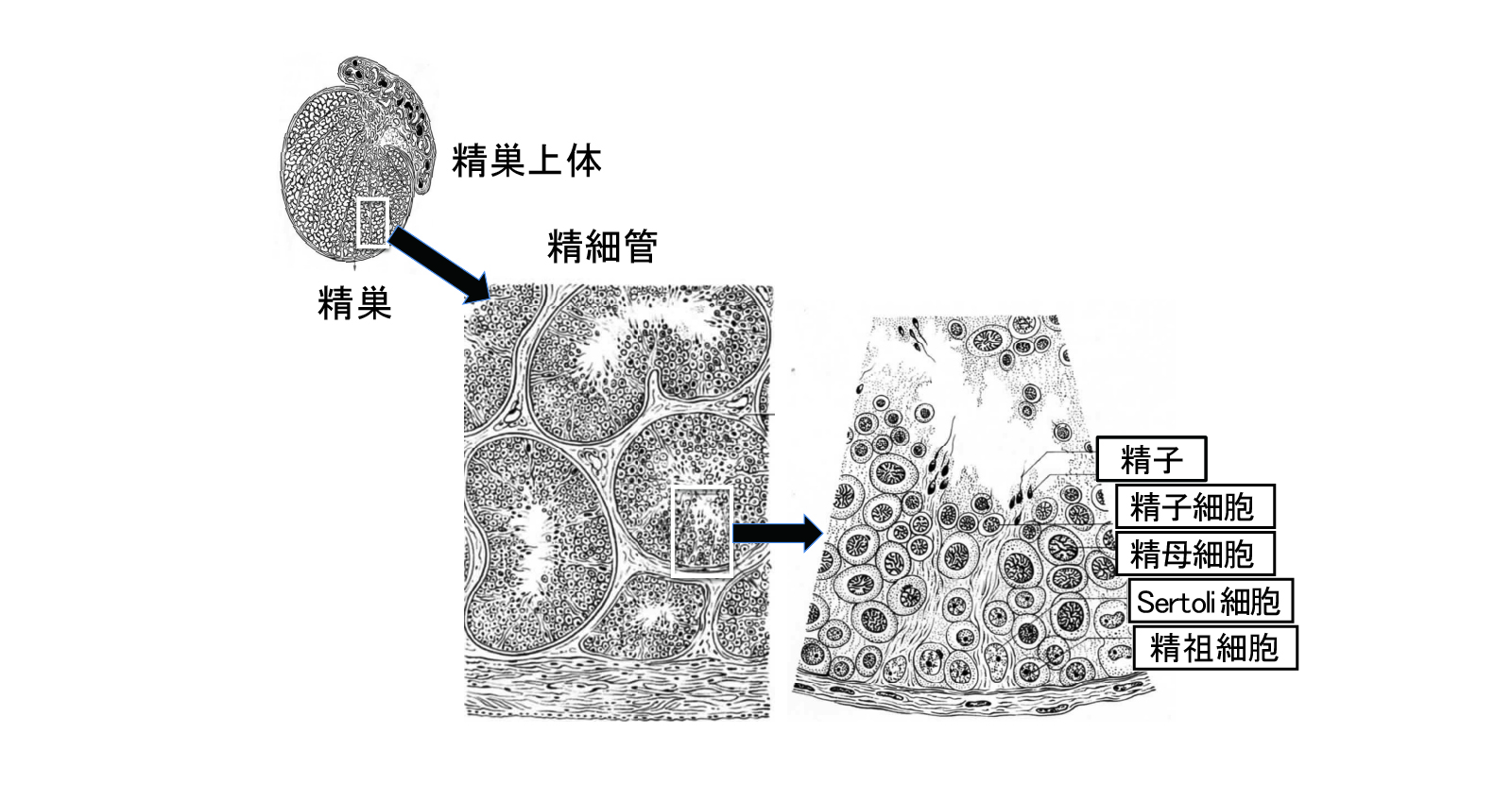
精巣は陰嚢の中にあり、内部には200μm程度の太さの精細管という管が600本程度入っています。精細管1本の長さは70-80cmで、1精巣あたり250m程度の長さになります。 精細「管」は管ですので中は空洞になっているのですが、管の中には壁(基底膜)に沿ってSertoli(セルトリ)細胞、精細胞といった細胞が存在します。Sertoli(セルトリ)細胞はその細胞内に精細胞を取り込み、これを支持しつつ栄養や分化に必要な物質を与え、増殖と分化を促しています(図1)。セルトリ細胞の機能は脳下垂体から分泌される卵胞刺激ホルモン(Follicle stimulating hormone :FSH)や精巣内のLeydig(ライディッヒ)細胞から分泌されるテストステロンによって制御されています。FSHの分泌が過剰になって精子を作り過ぎないようセルトリ細胞はインヒビン(Inhibin)という物質を産生し、これが脳の下垂体へ届くとFSHの産生が抑えられます。このようにして精子産生をうまく制御しているのです。
一方、そのセルトリ細胞に囲まれて存在する精細胞は精子になる細胞の集団です。精細管の一番内腔壁(基底膜)側から内腔に向かってSertoli細胞の間に存在しています。まだ分化していない精細胞は基底膜周辺に存在していますが、精子への分化が進むにつれセルトリ細胞によって内腔近くへと移動させられ、精子になって内腔へ放出されます。
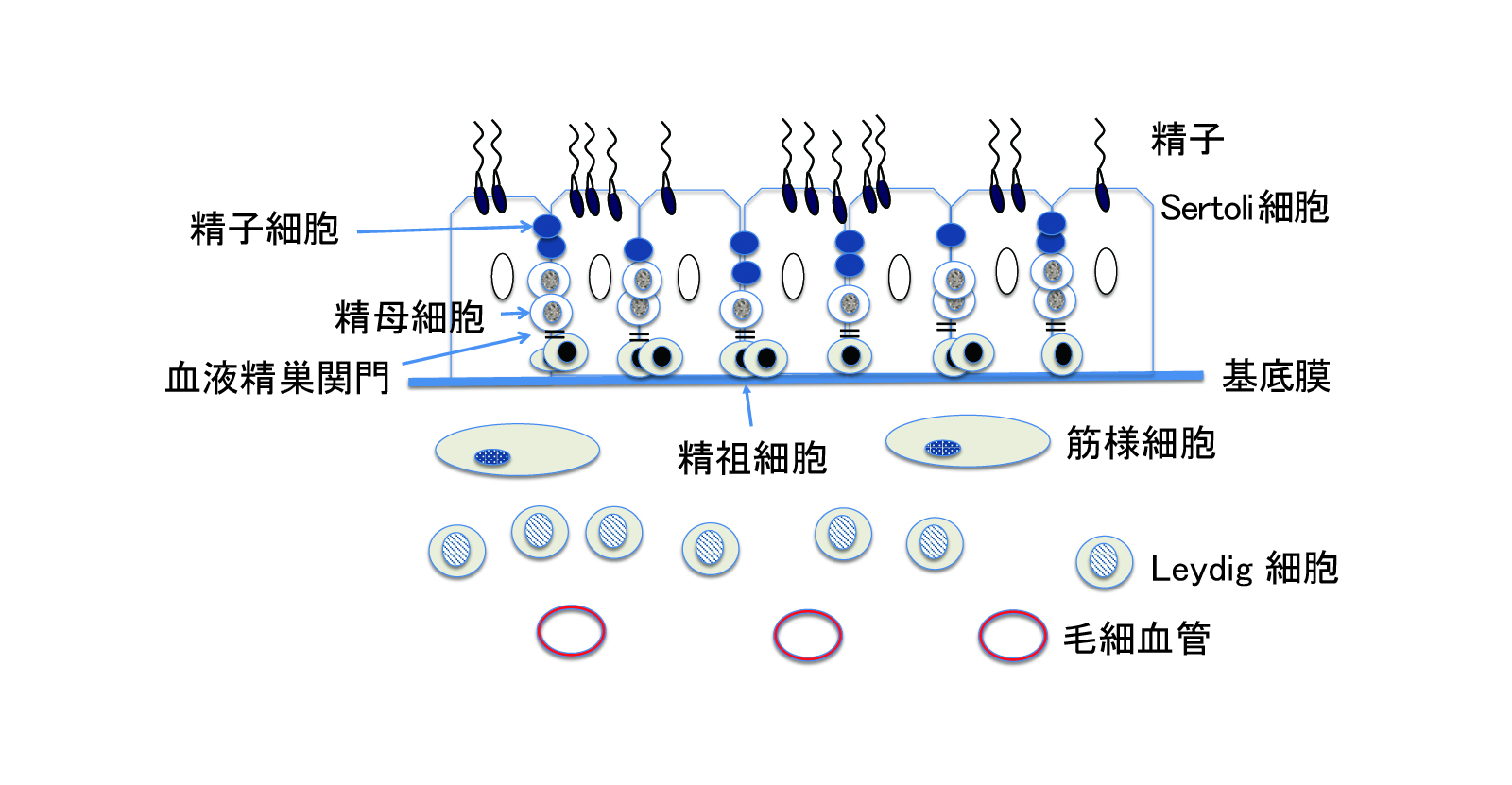
まだ分化していない精細管基底膜上に存在する精細胞は、精子の祖先ということで精祖細胞と呼ばれています。精祖細胞は、その数が減ってくると自分で分裂して数を増やす自己増殖機能と、精子への分化機能の両方を行うことができます(図2)。
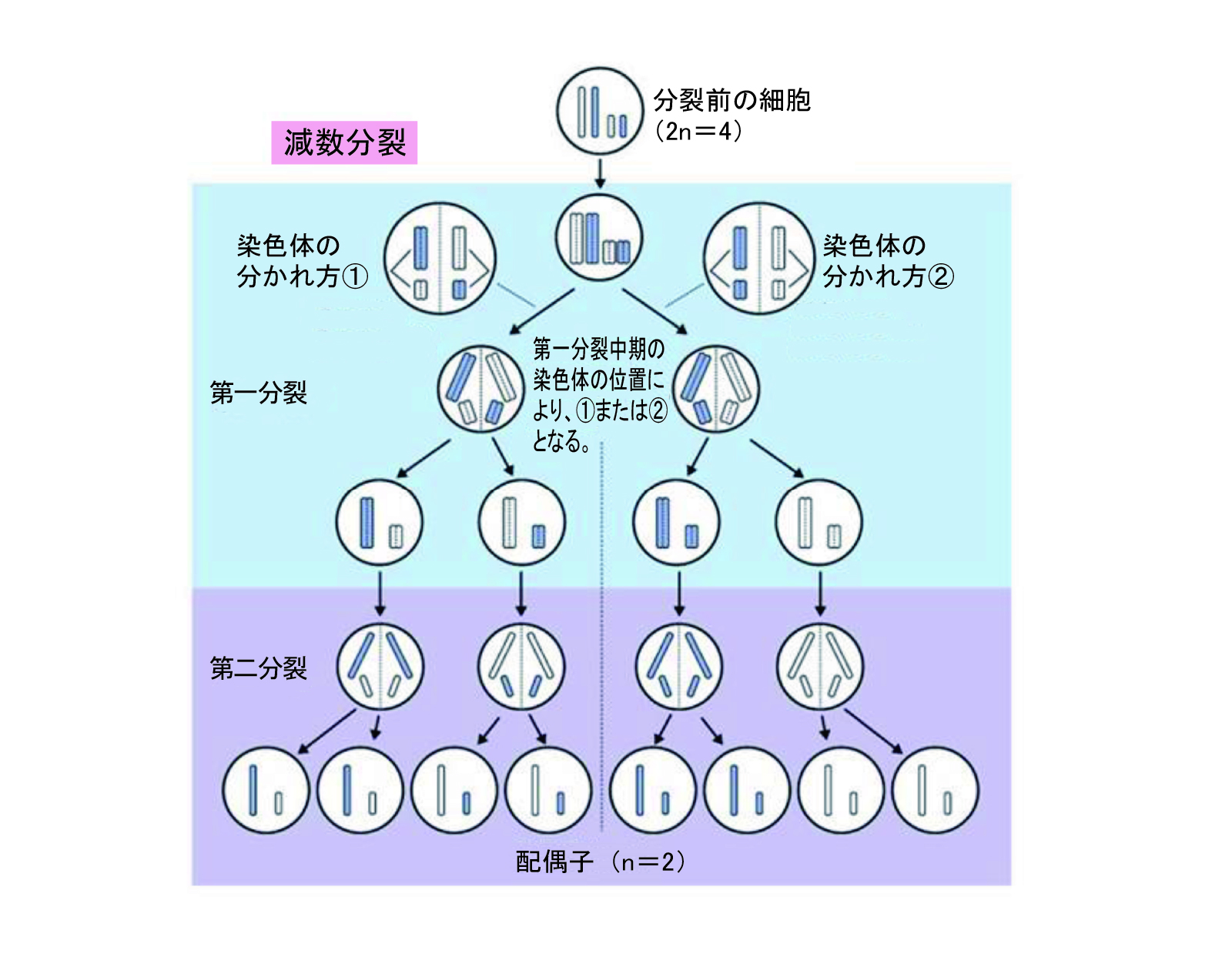
ところで精子と卵子が融合(受精)する場合、通常の細胞と同じ量の遺伝子(ここでは染色体)を持っていると出来上がる受精卵は遺伝子の量が二倍になってしまいます。そのため精子や卵子は完成する前に、その遺伝子の量を半分にするような細胞分裂を行います。これを減数分裂といいます。女性の場合卵子の減数分裂は胎児期に終了していますが、男性の場合、精子は思春期以降作られるのでこの精祖細胞が分化してゆく過程で減数分裂を行い、精母細胞を経て精子細胞と分化してゆく過程で遺伝子の量を半分にします(図3)。
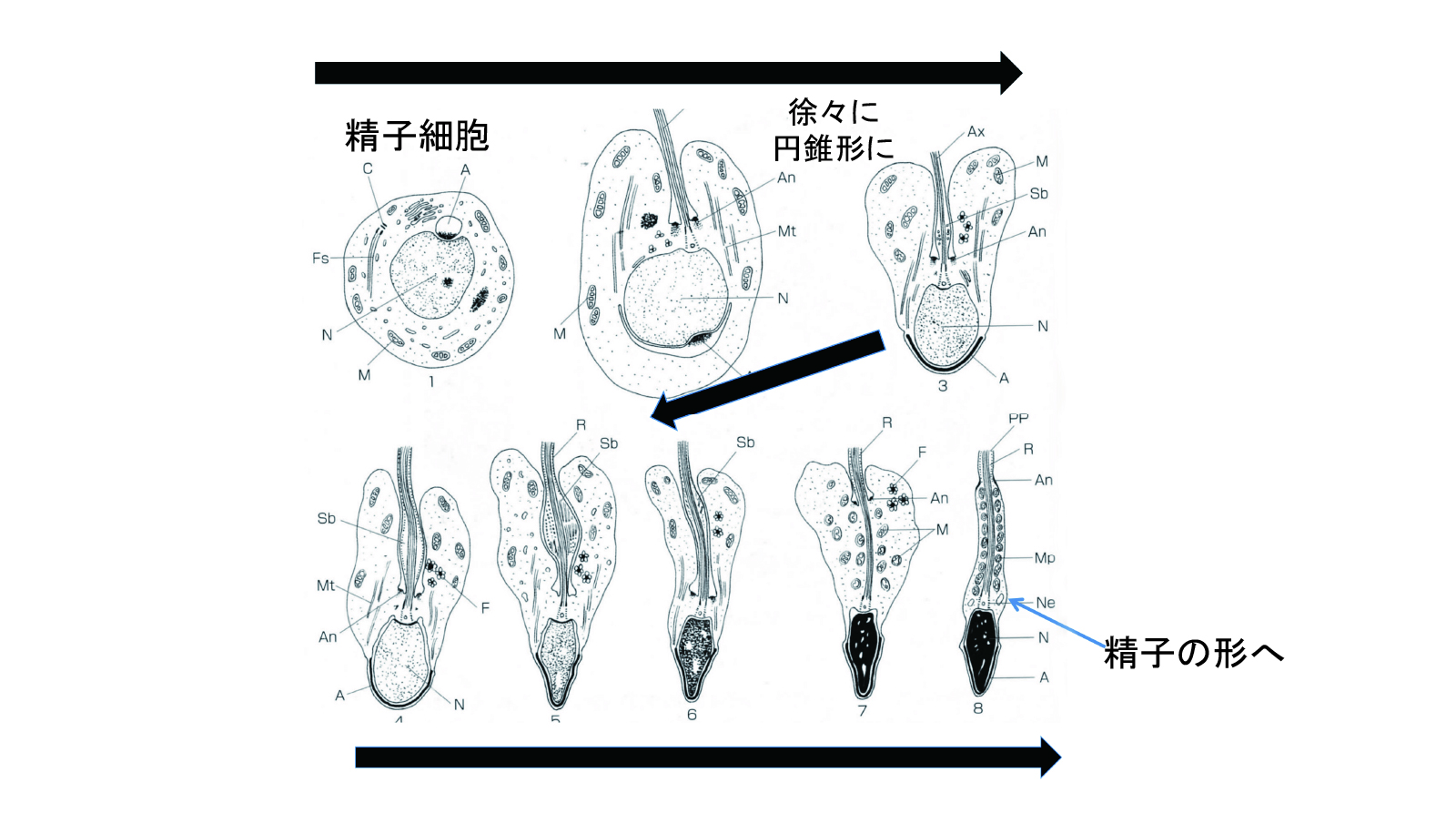
さて、精子細胞が出現したのでようやく精子ができた、と思う方もいらっしゃると思いますが、実は精子細胞と精子は異なります。この時点で精子細胞は丸い形をしていますので円形精子細胞と呼ばれることもあります。この円形の精子細胞が徐々に形を変え尾が生えてゆき、最終的にオタマジャクシのような精子の形になります(図4)。
精子の核内でも男性のDNAを運びやすいよう、しまい方を変えて出発の準備を整えます。細胞の位置も円形精子細胞の時にはセルトリ細胞間にいたものが、精子になると精細管の内腔に移動し、成熟できた時点でセルトリ細胞から切り離されて内腔へと放出されます。この時点での精子は動いていないか動いていても微動なのですが、精細管は周囲の筋肉様細胞の働きで内腔の精子を移動させることができます。この蠕動運動により精子は精巣網、輸出管を経て、精巣の外に出て精巣上体管へと進みます。精巣上体管の全長は4〜5m程度あり、ここで精子は成熟し、運動性を獲得して出発(射精)のときを待ちます。
従来精子の完成までに約74日を要すると考えられてきましたが、近年の研究では個人差があり、42〜76日と開きがあることが分かってきています。
性機能
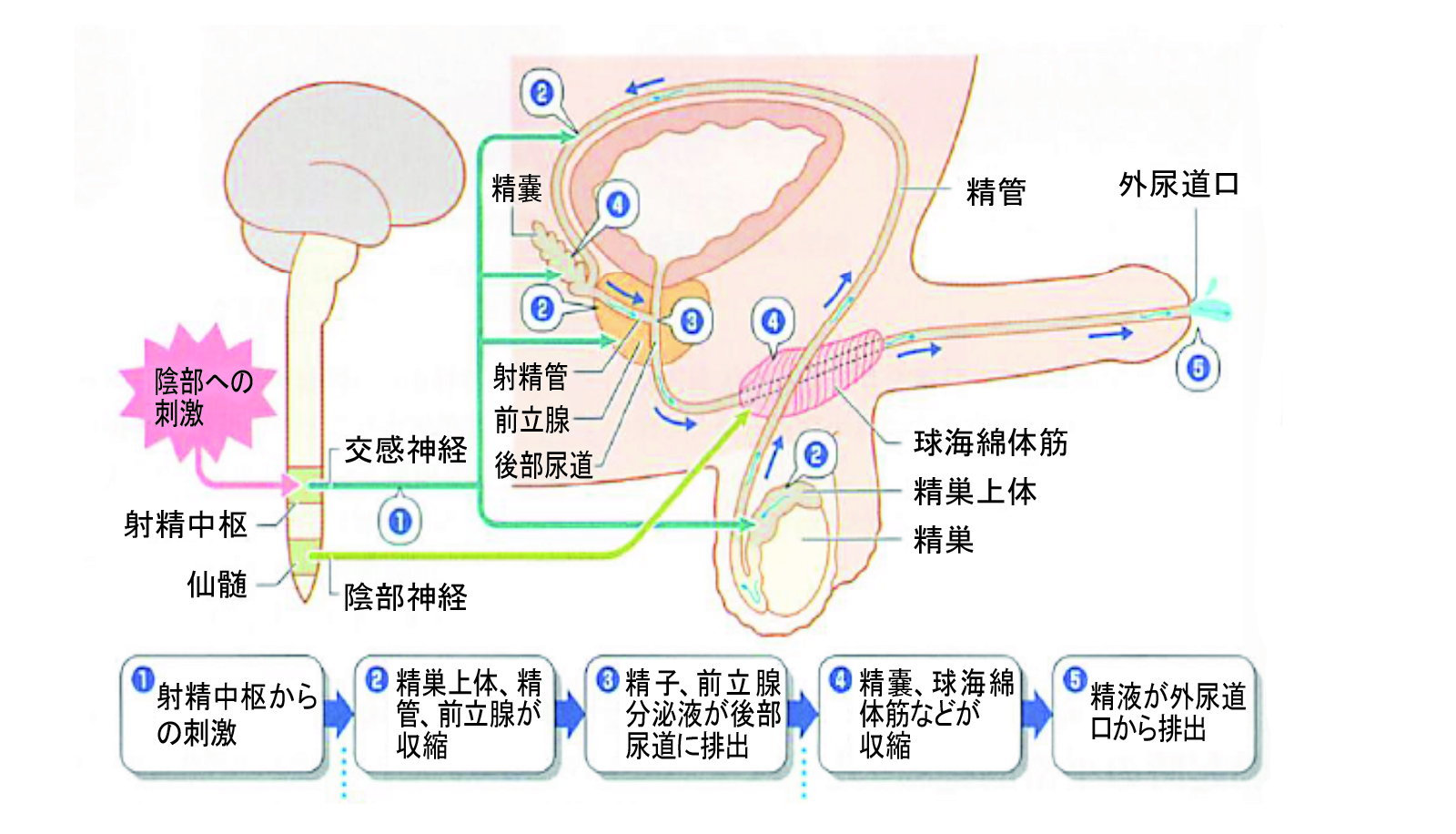
精子ができるまでをお話ししましたが、生殖機能のもう一つの工程でもある精子が体外に放出されるまでのお話をさせていただきます。いわゆる「射精」のお話です。射精は以下の三つの工程からなりたっています。
- 精嚢液、前立腺液と精子が混合して尿道へ排出される。
- その精液が体外へ排出される。
- 射精時の排尿と膀胱内への精液逆流をふせぐための内尿道口(膀胱の出口)が閉鎖される。
以上の三つの現象から射精という工程は構成されています。オーガズムを迎え、上記の工程を司るのは人間の神経の中で「交感神経」です。交感神経は自律神経の一つで体内の臓器をうまく機能させるために必要な神経です。交感神経は通常は交感神経幹という束になって大動脈の脇を走り各臓器に枝を出しています。交感神経が損傷するような事態(糖尿病や脊髄の損傷、大動脈周辺の手術など)によって射精ができなくなるケースもあります。
一方性機能にはもう一つ、重要な要素があります。それは勃起です。勃起は性的刺激を受けて性欲が発来して起こります。オーガズムの発来と射精後陰茎は弛緩する、という一連の過程を経ます。
勃起に必要な神経は「副交感神経」と呼ばれ、外界からの刺激に対して反応する自律神経系のひとつで、生体内のホルモンなどを制御しています。簡単に言えば、心身がリラックス状態の時に働く神経です。 そして、この「副交感神経」が男性機能への直接的な性的刺激、あるいは「視覚・聴覚・臭覚・味覚・触覚」などの性的な刺激を勃起中枢神経へ運ぶことで勃起が起ります(図5)。
さらに具体的に言うと、副交感神経により運ばれた性的な刺激は、勃起中枢神経に到着し、血管拡張物質である一酸化窒素(NO)が大量に分泌されることで、ペニス内の血管が広がって、血液が大量に海綿体に流れ込み、海綿体の静脈が締め付けられ充血状態となって、勃起状態を導きます。こちらも射精と同様に副交感神経が損傷するような事態(糖尿病など)や血管の流れが障害される事態などがあれば勃起できない状況、EDとなります。
また、勃起は副交感神経の制御ですので、緊張状態などではうまくいかない可能性があります。これは心因性のEDと呼ばれます。
横浜市立大学附属市民総合医療センター 生殖医療センター泌尿器科
湯村 寧
化学療法による精巣毒性のメカニズム
はじめに
若年性のがん患者の治療成績は、治療法の進歩に伴い非常に改善しています。しかし、その反面患者さんに対して行われる放射線治療や化学療法は、生殖細胞への毒性が高く、男性であれば精子形成能が低下し、男性不妊の原因となることが知られています。ではなぜ、抗がん剤は生殖細胞を傷害するのでしょう。
抗がん剤の多くは細胞の分裂時に細胞に何かしらのダメージを与え、分裂をさせないようにするというのが主な作用機序です。最も精細胞にダメージを与える抗がん剤である、シクロホスファミドに代表されるアルキル化剤では、DNAにアルキル基を付着させて細胞のDNA合成を阻害します。その他、DNAの鎖の間に介入してDNA合成を阻害する、DNAを切断する、細胞分裂時に出現する微小管の生成を阻害するなど、抗がん剤はいろんな方法で細胞の分裂を邪魔していきます。これによりがんの増殖は抑えられるわけですが、問題なのは抗がん剤が全身を回るため、この効果はがん細胞以外の健常な細胞にも及ぶことです。男性の場合、精細胞も例外ではありません。
精子形成の項でも書かせていただきましたが、精細管のなかで精子は作られています。この精細管には直接血管は入り込んではいません。精子形成に必要な物質は、精細管の周囲から精細管(セルトリ細胞)に取り込まれて精細胞や精子に届けられます。この時、有害な物質は精子へ届けないようにしようという作用も存在するのですが、残念ながら通過できる薬剤は多く、抗がん剤なども通過してしまいます。そして、精細管のもっとも外側にある精細胞である精粗細胞は、抗がん剤の効果に最も弱いとされています。
化学療法による精細胞への影響
精細管内で抗がん剤は精粗細胞、後期の精細胞への毒性を呈し、精子の数は治療開始から1〜2ヶ月で急激に低下していきます。もちろん、その間も生き残った精細胞から精子は作られているのですが、精子の遺伝子の損傷が強く、化学療法開始後数ヶ月の妊娠は避けるように言われています。治療後2ヶ月以上経過した場合、無精子症になることもあります。ただ、この場合の無精子症はずっと続く方もいれば、いずれ回復してくる方もいらっしゃいます。アメリカ臨床腫瘍学会(American Society Clinical Oncology: ASCO)は抗がん剤、放射線治療における精巣へのリスクを4つに分類しています(表)。ここでいうHigh risk とは「治療後一般的に無精子症が遷延する」治療、intermediate riskは「治療後無精子症が遷延・永続することがある」治療を指します。つまりintermediate riskの治療といえども無精子症をきたす可能性はあり、精子保存は行っておいた方が良いと思われます。また、low riskは「一過性の造精機能障害をきたす」治療であり、治療後精液所見が改善していく可能性はありますが、度重なる抗がん剤投与により、または治療前から精液所見が悪化していた場合には無精子症の遷延が生じることもあります。この表をみるとlow riskだから精子保存はしておかなくても大丈夫だな、と思ってしまう方もいらっしゃるかもしれないのですが、リスク分類のみで精子保存の判断を行うことは難しいとも言えます。
また、リスク分類の表をご覧になっていただけますとおわかりになると思いますが例えばシクロホスファミドは7.5g/㎡(ここでいう㎡は体表面積をさします。身長と体重から換算されます)、シスプラチンは400mg/㎡以上でリスクが上昇します。また精巣腫瘍に使われる多剤併用療法のBEPはシスプラチン、エトポシド、ブレオマイシンを使用しますが、2〜4コース以上で中間リスクとなります。このように精巣へのダメージは抗がん剤の総投与量が増すほど大きくなります。
また、近年、一般的な抗がん剤とは異なる機序で、がん細胞増殖を抑える薬剤が多数出現しています。分子標的剤と言われる薬剤です。細胞上に存在する分子を標的にしてそこに付着し、細胞増殖のシグナル抑制を行うことでがんを抑えていきます。抗がん剤との違いは、抗がん剤が数ヶ月間で細胞を殺すこと(殺細胞作用)に主眼を置いているのに対し、分子標的剤は何年も細胞をそのまま増殖させないようにすることに重きをおいている点です。細胞上の種々の分子については、がん細胞と同様の分子を精細胞が細胞表面に有していることも時々ありますが、だからといって必ずしも造精機能が低下するわけではないようです。逆に内服することで精子数が低下したという報告もあり、どの程度造精機能に効果があるのかはっきり分かっていません。しかし、見た目は問題なくても精子のDNAなどに問題はないのかも不明です。今後の研究が待たれます。
抗がん剤治療と造精機能の回復
「抗がん剤治療を行った場合、どの程度の時間をかけて造精機能は回復してくるのか?」これは、治療を行った患者さん皆が知りたいところだと思います。回復の度合いは、抗癌剤治療で生き残った精粗細胞がどの程度存在するのかで変わってきます。精粗細胞が生き残っていれば、その自己複製能力でまた精子を作り出すことが可能になります。殺細胞効果の少ない薬剤、もしくはその併用療法などでは精子の数は減少するものの、無精子症になることはなく3〜4ヶ月程度で回復します。反面、殺細胞効果の高い、High risk・intermediate riskの薬剤では無精子症を呈し、回復までに数年を要することもまれではありません。また、同じ抗がん剤でもその投与量が多ければ回復率は低下し、回復までの期間も遅れてしまいます。このような場合には、回復できない可能性も考えて精子の保存をしておいた方が良いということになります。
抗がん剤治療後の精子の回復
「がん治療が終わった後の精子で妊娠することは出来るのか?」「妊娠して大丈夫なのか?」これは、がん治療を行った若年の男性患者さんであれば、皆心配するところではないでしょうか。実はやはり抗がん剤治療を行った患者さんの精子は、染色体数の異常が多く見られるというデータがあります。おそらくですが、精子のDNAも損傷している可能性が高いと思われます。しかし、この現象は治療が終わって一定の期間が経過すると改善すると言われています。
例えば、精巣腫瘍の治療であるBEPの場合、コースの回数にもよりますが、染色体の数に異常をもつ精子の比率は24ヶ月で治療前の水準に戻ると言われています。また、悪性リンパ腫の治療ですとABVDで3ヶ月、CHOPで12ヶ月は治療前より比率は高いもののその後は低下していくと言われていますので、ある程度の時間をおけば治療前と変わらない精子の状況になると考えられます。抗がん剤の種類、レジメ、投与量によっても差はありますが精子が出現してきた場合、時間をおけば子作りを始めてもよいことになります。
横浜市立大学附属市民総合医療センター 生殖医療センター泌尿器科
湯村 寧
表 各治療の造精機能へのrisk (ASCO Clinical Practice Guideline 2013より)

精巣への放射線照射が生殖機能に及ぼす影響
はじめに
抗がん剤治療とならび放射線治療は現在、がん治療に必要不可欠な治療法です。しかし、放射線治療の副作用として抗がん剤と同様生殖細胞への毒性があり、男性であれば精子形成能が低下する可能性があります。
放射線によって細胞は細胞内のDNAを損傷させられます。また、同様に細胞内で酸素分子が不安定となり、活性酸素となってこれもDNAを損傷し、細胞は死に至ります。一気に大量の放射線を浴びると正常な細胞も死んでしまうので、これを分割して毎日少しずつ放射線を照射します。正常の細胞は修復力が高いので、DNAも含めて修復することができます。がん細胞の修復力は弱いため自己修復ができず細胞死にいたる、というのが放射線治療の機序です。
放射線が精子に与える影響
しかし、現在まで「完全に」がん組織のみに放射線を照射させるという技術はまだ確立していません。どんなに照射範囲を狭める努力をしても、残念ながらある程度の放射線は正常組織にもかかってしまいます。また、分割照射は現在の放射線治療の主流ではありますが、いかに通常細胞の修復力が高いと言っても、何回も繰り返し照射されれば死んでしまう細胞も出てきます。抗がん剤の項にも書かせていただきましたが、精細胞のうち特に最初の段階である精祖細胞は、放射線の殺細胞効果にもっとも弱いと言われています。また、照射されてもすぐに細胞は減少せず、主に精祖細胞から減数分裂途中の精母細胞までが照射後2週間程度で減少、精子は照射後10週間で劇的に減少するとされています。そして約18週以降には無精子症をきたす症例も現れます。
ではどのくらいの線量をあびると精細胞はダメージをうけるのでしょうか。文献的には30Gy〜70Gyを照射された場合、細胞内では遺伝子の異常が発生すると言われています。精細胞については単回照射で0.1〜0.2Gyの照射を受けた時から精祖細胞が減少し始め、4Gyで不可逆的なダメージを与えられ、4〜6Gyで精子の数はかなり減少します。また、男性ホルモンを産生しているLeydig(ライディッヒ)細胞も放射線照射によりダメージを受けることがわかっています。線量が上がれば無精子症を呈することもあります。
ところで今回記載されているGyという単位ですがグレイ、と読みます。よく皆さんが知っている放射線の単位でBq(ベクレル)やSv(シーベルト)がありますが、これとGyはどのような関係があるのでしょうか?これはよく聞かれる質問なのでいろいろなサイトや本に説明が掲載されています。
Bq(ベクレル)は放射性物質が放射線を出す能力を指します。Gy(グレイ)は放射線が1 kgの物質に与えるエネルギーの量(吸収線量)であり、Sv(シーベルト)は放射線が人体に及ぼすダメージを表わす量となります。GyとSvの関係だけ見ますと、Gyはエネルギー量なので体のどこに浴びても同じ量なのですが、Svは人体の臓器の種類によって変わってきます。例えば、皮膚や骨よりも精巣はとてもダメージを受けやすいので同じGyでもSvは異なるという現象が生まれます。臓器はそれぞれ与えられるダメージの係数が決まっていてSv=修正係数(臓器ごとに異なる)×Gyといわれています。
放射線治療における線量リスク
放射線による精細胞の減少は線量のほか、照射方法(単回照射か分割照射か)、照射の範囲によっても変わってきます。アメリカ臨床腫瘍学会(American Society Clinical Oncology: ASCO)は抗がん剤、放射線治療における精巣へのリスクを4つに分類しています(表)。このリスク分類は抗がん剤や多剤併用レジメの分類が有名ですが、放射線の線量のリスクも記載されています。例えば、精巣への照射でも線量が上がればそれだけリスクは高まってゆくことがわかります。また放射線照射単独ではなく、抗がん剤とくにアルキル化剤と精巣を含む骨盤照射や全身照射はかなり強力なダメージとなり、High risk groupに分類されています。
白血病などで骨髄移植の準備としてアルキル化剤と全身照射が行われますが、多くの患者さんで無精子症が遷延します。このような患者さんに対し、治療終了後に顕微鏡下精巣内精子回収術を行うことがありますが、ほとんど精子は回収できません。また、骨盤照射とアルキル化剤の組み合わせも無精子症を来すリスクの強い治療です。このような患者さんには治療前の精子凍結を行っておくべきだと思われます。
また、精巣へのダメージとは異なりますが、脳への照射により視床下部や下垂体と言ったホルモンを分泌する組織にダメージが生じると、脳下垂体から分泌される卵胞刺激ホルモン(Follicle stimulating hormone :FSH)の分泌が低下し、精子の産生が障害されることもあります。この場合、同時に下垂体から分泌されるテストステロン産生に関与する黄体ホルモン(LH)の分泌も低下しているためテストステロンも低下し、小児であれば二次性徴の遅延、成人であれば精液量の減少、無精子症なども見られる場合があります。診断が付けばFSHやLHの補充療法で治療が可能です。
放射線量と造精機能回復の関係
「放射線治療後どの程度の時間で造精機能は回復してくるのか?」これは抗がん剤治療と同様、生き残った精粗細胞がどの程度存在するのかで変わってきます。精粗細胞が生き残っていれば、その自己複製能力でまた精子を作り出すことが可能になります。線量が少なければ、殺細胞効果も少ないため早めに造精機能は回復していきますが、それでも1Gyの照射後だと7ヶ月後から回復は始まり、治療前の水準に戻るには2年を要すると言われています。これが6Gyの照射だと回復し始めるのは照射後24ヶ月を経過してからとされており、抗がん剤よりも時間を要することになります。10Gyを超える照射になると無精子症を呈する患者が高率に出てくると言われています。その割合は文献によって異なるようです。
ここまでは一回の照射でのお話しが主でした。しかし、単回照射は他の細胞へのダメージが大きいので、患者さんへの副作用軽減のため照射野の縮小とともに分割照射が多く行われています。にもかかわらず、分割照射は造精機能の回復を遅らせる、低い線量でも何度もかければ無精子症になりやすい、と言われています。いずれにせよ、高い線量を精巣に照射する場合は予防的に精子の保存は行っておいた方が良さそうです。
横浜市立大学附属市民総合医療センター 生殖医療センター泌尿器科
湯村 寧
表 各治療の造精機能へのrisk (ASCO Clinical Practice Guideline 2013より)

精子凍結
この内容については準備中です。
妊孕性の予後
この内容については準備中です。




